دراسة تكشف كيف تبطئ أحد أدوية السكري الشائعة من نمو الخلايا الطبيعية التي تحمل طفرة التحول إلى السرطان
تقترح دراسة جديدة أن الميتفورمين، وهو دواء شائع لمرض السكري، يبطئ نمو الخلايا السابقة للسرطان في المريء بينما تسرع بعض الحالات الاستقلابية من هذا النمو.
واكتشف باحثون من معهد ويلكم سانجر (Wellcome Sanger) أن الميتفورمين قلل من نمو الخلايا القابلة للتسرطن في الفئران والتجارب المخبرية. ووجد الفريق أيضًا أن الحالات الاستقلابية مثل السكري والسمنة يمكن أن تعزز ميزة نمو هذه الخلايا المتغيرة في عينات البشر.
وتبرز النتائج التي نُشرت مؤخرًا في مجلة ناتشر جينتكس (Nature Genetics) دور الميتفورمين المحتمل والصحة الاستقلابية العامة في إدارة خطر سرطان المريء. ويقترح الباحثون أن الدواء قد يكون مفيدًا خارج دوره في السكري، على الرغم من أن هناك حاجة إلى المزيد من البحث.
يُشخص حوالي 9,200 حالة سرطان مريء جديدة في المملكة المتحدة كل عام، ونحو خُمس هذه الحالات هي سرطان الخلايا الحرشفية. ولدى المرضى نسبة نجاة ضعيفة، وفي إنجلترا فقط حوالي 17 بالمائة من هؤلاء يبقون على قيد الحياة لمدة خمس سنوات أو أكثر. وتنشأ هذه الأورام من خلايا محورة موجودة في المريء.
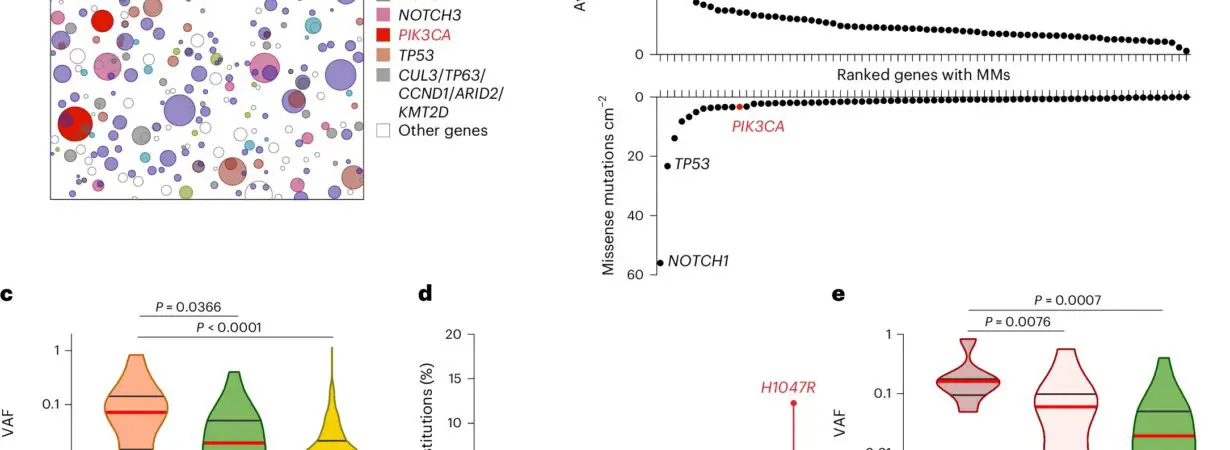
ومع تقدمنا في السن، تتراكم تغيّرات جينية طبيعيًا في خلايا أجسامنا. بينما تكون معظمها غير ضارة، يمكن لبعضها منح الخلايا ميزة نمو وقد تؤدي مع الوقت إلى الأمراض المرتبطة بالعمر مثل السرطان. ويُعرف أن الجين المسمى PIK3 CA بأنه يلعب دورًا رئيسيًا في نمو الخلية. وعندما تحدث تحورات في هذا الجين، تُسبب تكاثر الخلايا بسرعة، ويمكن أن تؤدي إلى سرطان المبيض، والثدي، والرئة، والدماغ، والمريء.
في هذه الدراسة الجديدة، استخدم الباحثون من معهد ويلكم سانجر التجارب في الفئران وأساليب زراعة الخلايا وتسلسل الحمض النووي في عينات البشر لدراسة تطور التحورات في المريء. وكان تركيزهم على تحور معين في الجين PIK3 CA يمكن أن يدفع الخلية للنمو العنيف في حالة التغيير.
ولاحظ الفريق أن الخلايا ذات التحورات في PIK3 CA تنمو بسرعة أكبر من الخلايا الطبيعية. ووجدوا أيضًا أن اتباع نظام غذائي عالي الدهون والسكري من النوع الأول في الفئران يُعززان نمو الخلايا ذات تحورات PIK3 CA. وعندما فحصوا عينات المريء البشرية، وجدوا أن لدى الأشخاص الذين يعانون من زيادة الوزن المزيد من الخلايا ذات تحورات PIK3 CAمقارنة بأولئك ذوي الوزن الطبيعي، مما يدل على أن السمنة قد تزيد من خطر الإصابة بسرطان المريء.
وعلى الجانب المقابل، اكتشفوا أن عند معالجة الخلايا المتحورة بدواء مكافحة داء السكري الميتفورمين، فإن الخلايا المتحورة تفقد ميزتها في النمو، سواء في الفئران أو في الخلايا المزروعة في المعمل. وشوهد هذا التأثير في الفئران غير المصابة بداء السكري.
ويعد الميتفورمين الدواء الأكثر شيوعًا في وصفه للأشخاص الذين يعانون من السكري من النوع الثاني، ويُستخدم لعلاج المستويات العالية من السكر في الدم. وأشارت الدراسات الوبائية السابقة إلى أن الميتفورمين قد يقلل من حدوث السرطان في السكان الذين يعانون من السكري، لكن الآليات الدقيقة للعمل والفئات التي قد تستفيد منها لم تكن مفهومة فهمًا جيدًا.
إن تأثير الميتفورمين على نمو الخلايا الحاملة لتحورات PIK3 CAيفتح الباب لإعادة توجيه استخدام هذا الدواء لمنع السرطانات ذات الصلة بتحورات PIK3 CA.
“مع تقدمنا في العمر، تتراكم خلايانا المتحورة. وتفتح معرفة العوامل التي تدفع الخلايا التي تحمل هذه التحورات المرتبطة بالسرطان إلى النمو بوقت طويل قبل تطور السرطان الباب أمام استراتيجيات جديدة للوقاية. وهذا يسلط الضوء على كيف يمكن للتقدم في علم الخلايا أن يؤدي إلى فوائد صحية غير متوقعة.
ويقول الدكتور ألبرت هيرمس: “مع المزيد من الوعي حول ما يحرك السرطان، هناك فرص متزايدة لإعادة استخدام الأدوية القائمة، واكتشاف علاجات جديدة، واستكشاف تغييرات في أساليب الحياة التي يمكن أن تقلل من خطر السرطان”.
ويقول الدكتور فيل جونز: “تبين نتائجنا كيف يمكن استخدام دواء شائع وآمن مثل الميتفورمين بطرق جديدة لمنع السرطانات ذات التحورات PIK3 CA. ويُمكن لهذا الاكتشاف أن يقدم أداة جديدة للوقاية من السرطان، خاصة في الأشخاص المعرضين لمخاطر أعلى بسبب الاضطرابات الاستقلابية”.
“واحدة من أسرع الطرق لتحسين نتائج السرطان هي العثور على استخدامات جديدة للأدوية القائمة”.
ويمنحنا هذا البحث نظرة أولية هامة إلى الطرق التي يمكن استخدام ميتفورمين فيها لمنع سرطان المريء، على الرغم من أنه يحتاج إلى مزيد من التجارب السريرية لفهم كيفية إعطائه، ومن هم المرضى الذين يمكن أن يستفيدوا أكثر.
“هذا البحث، ومشاريع مماثلة له، تقودنا نحو مستقبل مثير إذ يمكن أن يكون السرطان أكثر قابلية للوقاية” كما يقول الدكتور إيان فولكس.
- ترجمة: ياسمين البديوي
- تدقيق علمي ولغوي: رنا حسن السوقي
- المصادر: 1