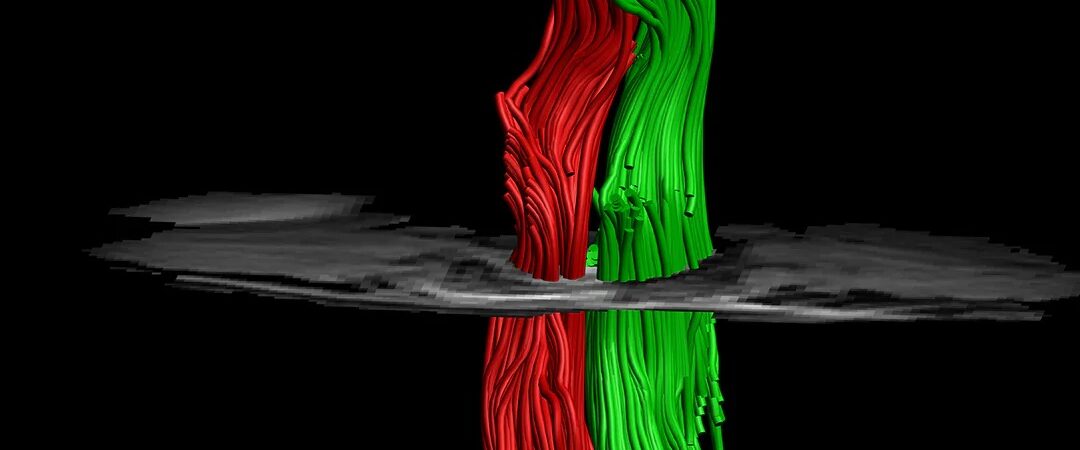
زراعة الحبل الشوكي تمكن الفئران من المشي مجددًا
تستخدم زراعة الحبل الشوكي لعلاج حالات انقطاعه مقدمةً الأمل بأن يصبح هذا النوع من الإصابات قابلًا للشفاء.
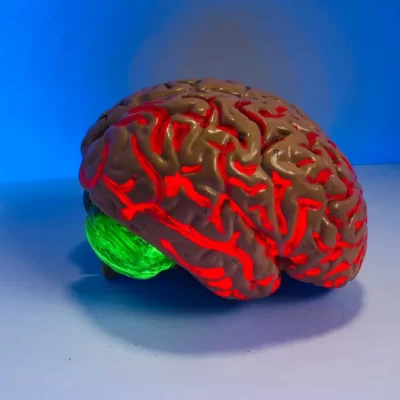
يمكن أن يكون لرض وأذية النخاع الشوكي تأثيرات مفصلية في الحياة. في حين أن درجة الخطورة تختلف تبعًا للإصابة الأولية، فكلما كانت الأذية أشد، كان الإنذار أسوأ وكانت الخيارات العلاجية الفعالة أقل. لكن المستقبل يبدو أكثر إشراقًا مع قيام فريق من الباحثين من جامعة تل أبيب بتغطية عملية جديدة لزراعة الحبل الشوكي تساعد في إعادة نمو الأنسجة العصبية المتضررة.
أوضح تال دفير، أستاذ التكنولوجيا الحيوية في جامعة تل أبيب والمؤلف الممثل للدراسة، في اتصالٍ أُجري معه: «هناك ملايين الأشخاص المشلولين حول العالم، ما نقوم به هو تطوير منهجيات هندسة الأنسجة للسماح لهم بالسير مرة أخرى».
غالبًا ما تؤدي إصابة النخاع الشوكي إلى موت الخلايا في تلك المنطقة وتشكيل نسيج ندبي. وبينما تستمر الأنسجة السليمة حول منطقة الإصابة في محاولة إصلاح الضرر عن طريق إرسال إشارات بيولوجية، إلا أن كل مساعيها تضيع سدى. لا تستطيع الخلايا العصبية الجديدة أن تنمو ولايسمح النسيج الندبي -الذي يتكون في المرحلة المزمنة من الإصابة- باندماج خلايا جديدة.
قال دفير: «عندما نتحدث عن ضرر النخاع الشوكي، فإننا نتحدث عن قطع أو اضطراب في النخاع نفسه، ولا تمر الأعصاب عبر النسيج الندبي المتشكل لاحقًا».
كان لمختبر ديفر سنوات من الخبرة في هندسة الأنسجة، وأبرزها الطباعة ثلاثية الأبعاد للقلب باستخدام خلايا المريض الذاتية في عام 2019. أوضح دفير: «هنا، استخدمنا نفس النهج الذي استخدمناه عندما أنشأنا القلب».
«في تلك الدراسة، قمنا بمحاكاة تطور أنسجة القلب. الآن، قمنا بالشيء ذاته باستثناء محاكاة تطور الحبل الشوكي. كان الاختلاف آنذاك من ناحية أننا قمنا بطباعة القلب، أما هنا فقد أنشأنا أنسجة أصغر للزراعة».
تختلف استراتيجية الفريق عن الأساليب الحالية التي تستخدم العلاج الخلوي في محاولة إصلاح ضرر النخاع الشوكي. وبينما تحقن تقليديًا أنواع مختلفة من الخلايا أو المواد الحيوية في موقع الإصابة على أمل أن تتكاثر هذه الخلايا وتنمو من تلقاء نفسها داخل الجسم، تنمو زرعات النخاع الشوكي الجديد مسبقًا في المختبر.
قال دفير: «تكون الخلايا المحقونة معزولة وبحاجة تكوين شبكة عصبية والاندماج مع الأنسجة السليمة».
«في مختبرنا، نهندس هذا النسيج لتشكيل الشبكة في طبق، ونقوم بزرعها فقط بعد أن يكتمل تشكيل شبكة عصبية ثلاثية الأبعاد. الشيء الوحيد الذي يتوجب على هذه الخلايا القيام به في الجسم هو الاتصال بالأنسجة السليمة، وهو أمر سهل جدًا».
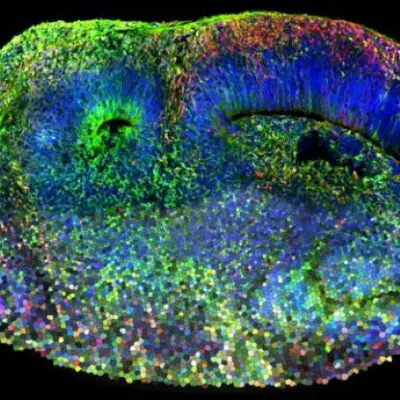
تُشكّل غرسة الحبل الشوكي عن طريق محاكاة نفس العمليات التي تحدث في أثناء التطور الجنيني للنخاع الشوكي، إذ توفر بيئة مجهرية ثلاثية الأبعاد مهندسة للخلايا النامية الرسائل والإشارات البيولوجية المناسبة لتشكيل نسيج جديد.
وتجنّب الفريق -الذي ضم طالب الدكتوراه ليور فيرتهايم والدكتور رؤوفن إدري والدكتورة يونا جولدشميت- خطر رفض الزرع كنتيجة لاستجابة الجسم المناعية الطبيعية باستخدام الخلايا والمواد المأخوذة مباشرة من المريض. أوضح دفير: «من خلال خزعة صغيرة، نأخذ الأنسجة الشحمية من معدة المريض ونعزل الخلايا والمطرق خارج الخلوي». ثم يعاد برمجة الخلايا باستخدام الهندسة الوراثية لتصبح ما يسمى بالخلايا الجذعية متعددة القدرات، والتي تشبه الخلايا الجذعية الجنينية تمامًا.
يمكن اعتبار الخلايا الجذعية متعددة القدرات بمثابة ألواح فارغة أو حتى خلايا رئيسية، لها القدرة على إنتاج أي خلية أو نسيج في الجسم. استخدمها العلماء جنبًا إلى جنب مع المطرق خارج الخلية المستخلص -شبكة ثلاثية الأبعاد من الجزيئات، مثل الكولاجين والمعادن والبروتينات السكرية المختلفة، التي تشكل الهيكل والدعامة للأنسجة الضامة في جميع أنحاء الجس – لإنشاء ما يسميه دفير «هيدروجيل شخصي» لغرسات النخاع الشوكي.
وأوضح: «نضع الخلايا الجذعية داخل هذه الهيدروجيلات ونضيف الجزيئات التي تفرز في الجنين لتشكيل الحبل الشوكي».
«نضيف هذا إلى وسط الزرع، أي إلى الأنسجة، في أثناء نموها للحث على تمايز الخلايا. يضمن ذلك أنها ستصبح «نخاعًا شوكيًا». نقوم بنفس الفعل الذي تقوم به الأجنة، لكن في طبق بتري».
لإثبات قدرة الغرسة على إحداث التئام في النخاع المتضرر، زرعها الفريق في فئران كان لديها قطع نصفي كامل في الجانب الأيسر في فقرة واحدة، مع بقاء الجانب الأيمن سليمًا. قارنوا نتائجهم بالفئران التي تلقت حقنة من الخلايا ووجدوا أنه بعد قرابة أسبوع، كانت الخلايا داخل مجموعة الزرع مرئية بوضوح في موقع الضرر، في حين أن تلك التي طُبقت عن طريق الحقن دون الزرع لم تُلاحظ إلا بصعوبة. وهذا يؤكد، وفقًا للفريق، على أهمية البيئة الداعمة في تجديد الأنسجة المتضررة.
وأضاف دفير: «أحد الأشياء الرائعة في هذه النتائج هو أننا لم نطبق الغرسة مباشرةً بعد الإصابة، وإنما في وقت لاحق في المرحلة المزمنة. هذا النموذج أكثر ملائمةً للتطبيق السريري لأن قلة من الناس سيحصلون على هذا العلاج فور الإصابة».
وأضاف: «لقد تمكنا بعد كل هذا الوقت (ما يعادل ستة أشهر إلى عام للبشر)، من إثبات أن هذه العملية ناجحة، ويمكن للحيوانات فعلًا المشي مرة أخرى».
«لقد أنشأنا شركة منذ عامين على أساس هذه التقنية ونعمل الآن على إحضارها إلى العيادة من أجل علاج المصابين بالشلل. آملين أنه في غضون عامين سنكون في التجارب السريرية».
- ترجمة: يارا خضور
- تدقيق علمي ولغوي: بهاء كاظم
- المصادر: 1