مصدر دمنا قد يكون غير معروف حتى الآن!
إن أجسامنا معقدة للغاية، لدرجة أن أكثر الأجهزة الحيوية المدروسة جيداً لم تزل تفاجئنا.
كشفت دراسة حديثة -أجريت على الفئران- أن الدم قد لا يكون له أصل خلوي واحد في الثدييات، بل أصلان.
قال فرناندو كامارغو، العالم البيولوجي في جامعة هارفارد وأحد الباحثين في دراسة الفئران، «آمن الناس أن معظم خلايا دمنا تأتي من عدد قليل جدًا من الخلايا التي تصبح لاحقًا خلايا جذعية دموية، المعروفة بالخلايا الجذعية المولدة للدم. ولكننا فوجئنا بوجود مجموعة أخرى من الخلايا السلفية التي لا تنشأ من الخلايا الجذعية. وهي تكوّن معظم الدم في الحياة الجنينية وحتى الفترة المبكرة من البلوغ، وبعدها تبدأ بالتراجع». وتعرف هذه الخلايا باسم السلائع الجنينية متعددة القدرات (eMPP).
تتشكل الخلايا الجذعية المولدة للدم في مرحلة باكرة من الخلايا المبطنة للشرايين. وكان يعتقد سابقًا أن eMPPs تنفصل عن الخلايا الجذعية المولدة للدم في مرحلة ما مبكراً في أثناء تطورها.
ولكن باستخدام إستراتيجية الترميز الجيني التي طورت مؤخرًا، تمكّن عالم الطب الحيوي بجامعة هارفارد ساشين باتيل وزملاؤه من تتبع الخلايا المنقسمة لرؤية أن الخلايا الجذعية المولدة للدم وeMPPs نشأت من نفس البطانة.
لإنجاز ذلك، دمج الباحثون أجزاء من تسلسلات الحمض النووي الريبوزي منقوص الأكسجين سهلة التتبع في مكان معين داخل جينوم خلية الفأر، حيث ستمرر هذه الأجزاء إلى جميع سلالاتها الخلوية. فأتاح لهم ذلك تتبع أصول جميع الخلايا المستهدفة، ليكشفوا أن eMPPs تنقسم إلى خلايا مسؤولة عن معظم الخلايا اللمفاوية (نوع معين من الخلايا البيضاء) في الفئران النامية. ويبدو أن خلايا eMPP هذه هي أمهات للعديد من الخلايا المناعية في الدم، بما في ذلك خلايا الدم البيضاء (الخلايا البائية والتائية).
وفي حين أن الخلايا الجذعية المولدة للدم يمكنها أيضًا إنتاج هذه الخلايا المناعية (كما هو موضح في النموذج أدناه)، فإنها تفعل ذلك بطريقة محدودة للغاية. إذ تميل إلى إنتاج المزيد من الخلايا التي تؤدي إلى تكوين أجزاء الدم الناشئة من خلايا النواءات- الخلايا التي تصنع المكونات اللازمة لتخثر الدم.
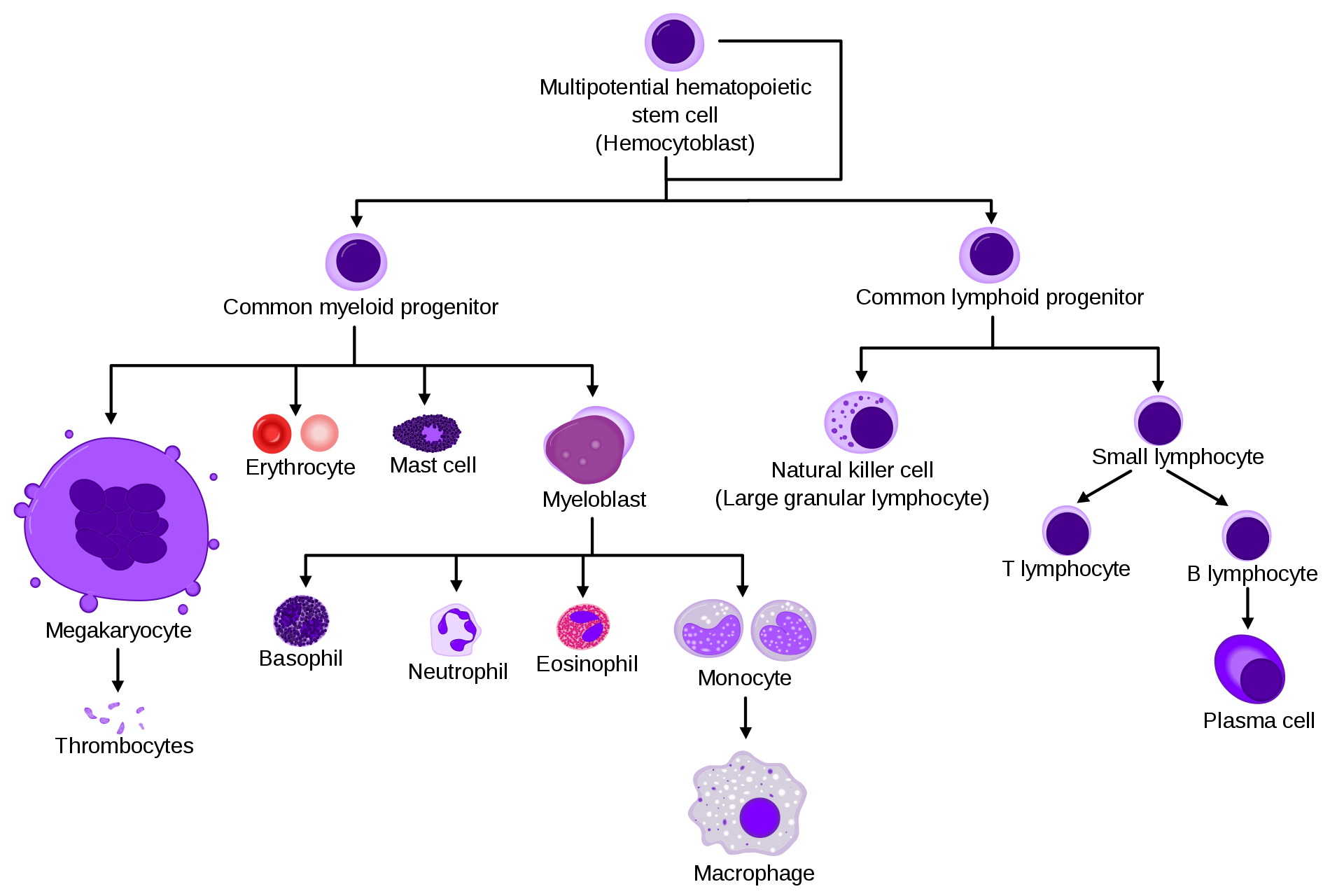
قال كامارغو «نحن نتابع لمحاولة فهم عواقب الطفرات التي تؤدي إلى ابيضاض الدم (اللوكيميا)، من خلال النظر في آثار هذه الطفرات في كلا خلايا الدم الجذعية وخلايا eMPPs في الفئران، نريد أن نرى ما إذا كانت ابيضاضات الدم الناشئة من هذه الخلايا مختلفة الأصول متفاوتة- أي أهي لمفاوية أم نقوية»
علاوة على ذلك، يبدو أن مساهمة eMPPs في إمداد الدم تتضاءل بمرور الوقت، مما قد يفسر اللغز القديم لسبب ضعف جهاز المناعة لدينا مع تقدمنا في العمر.
واختبر باتل وفريقه أيضًا كيف يمكن لهذه المعرفة الجديدة أن تحسن عمليات زرع نقي العظم، ووجدوا أن عمليات زراعة خلايا eMPP لم تدم جيدًا في الفئران. وأوضح كامارغو: «إن كان بإمكاننا إضافة عدة جينات للحصول على eMPPs طويلة الأجل لكان المحتمل أن تكون مصدرًا أفضل لزراعة نقي العظام. وخلايا eMPP أكثر شيوعًا في متبرعي النقي الأصغر سنًا من الخلايا الجذعية الدموية، وهي مهيأة لإنتاج الخلايا اللمفاوية، والتي يمكن أن تؤدي إلى إعادة تكوين الجهاز المناعي بنحو أفضل، إضافة إلى تقليل مضاعفات العدوى بعد التطعيم»
بالطبع، كل هذا لن يطبق إلا إذا كانت النتائج مشابهة لما يحدث في البشر. فلا تتقاطع دائماً السبل التطورية بين مختلف أنواع الثدييات. ويختبر الفريق حاليًا هذه الخلايا الجذعية الدموية في البشر ويأملون أن تؤدي نتائجهم إلى علاجات جديدة لتحفيز الأجهزة المناعية الهرمة.
- ترجمة: يارا خضور
- تدقيق علمي ولغوي: موسى جعفر
- المصادر: 1